- ปฏิกิริยาเคมีคืออะไร?
- การเปลี่ยนแปลงทางกายภาพและเคมีในเรื่อง
- ลักษณะของปฏิกิริยาเคมี
- ปฏิกิริยาเคมีแสดงอย่างไร?
- ประเภทและตัวอย่างปฏิกิริยาเคมี
- ความสำคัญของปฏิกิริยาเคมี
- ความเร็วของปฏิกิริยาเคมี
เราอธิบายว่าปฏิกิริยาเคมีคืออะไร ประเภทที่มีอยู่ ความเร็ว และลักษณะอื่นๆ อีกทั้งการเปลี่ยนแปลงทางกายภาพและทางเคมี
ปฏิกิริยาเคมีคืออะไร?
ปฏิกิริยาเคมี (เรียกอีกอย่างว่า การเปลี่ยนแปลงทางเคมี หรือ ปรากฏการณ์ทางเคมี) เป็นกระบวนการทางอุณหพลศาสตร์ของการเปลี่ยนแปลงของ วัตถุ. สองคนหรือมากกว่ามีส่วนร่วมในปฏิกิริยาเหล่านี้ สาร (รีเอเจนต์หรือสารตั้งต้น) ซึ่งเปลี่ยนแปลงอย่างมีนัยสำคัญในกระบวนการ และสามารถบริโภคหรือปล่อยได้ พลังงาน เพื่อสร้างสารตั้งแต่ 2 ชนิดขึ้นไปเรียกว่า สินค้า.
ปฏิกิริยาเคมีทุกเรื่องมีความสำคัญต่อการเปลี่ยนแปลงทางเคมี การเปลี่ยนแปลงโครงสร้างและองค์ประกอบโมเลกุล (ไม่เหมือนกับ การเปลี่ยนแปลงทางกายภาพ ที่ส่งผลต่อรูปร่างเท่านั้นหรือ สถานะของการรวมตัว). การเปลี่ยนแปลงทางเคมีโดยทั่วไปจะทำให้เกิดสารใหม่ ซึ่งแตกต่างจากที่เรามีในตอนแรก
ปฏิกิริยาเคมีสามารถเกิดขึ้นได้เองตามธรรมชาติ (โดยปราศจากการแทรกแซงของมนุษย์) หรือมนุษย์สามารถสร้างขึ้นได้ในห้องปฏิบัติการภายใต้สภาวะควบคุม
วัสดุหลายชนิดที่เราใช้เป็นประจำทุกวันได้มาจากทางอุตสาหกรรมจากสารที่ง่ายกว่ารวมกันผ่านปฏิกิริยาเคมีหนึ่งปฏิกิริยาหรือมากกว่า
การเปลี่ยนแปลงทางกายภาพและเคมีในเรื่อง
การเปลี่ยนแปลงทางกายภาพของสสารคือสิ่งที่เปลี่ยนแปลงรูปร่างโดยไม่เปลี่ยนแปลงองค์ประกอบ กล่าวคือ ไม่มีการดัดแปลงประเภทของสารที่เป็นปัญหา
การเปลี่ยนแปลงเหล่านี้เกี่ยวข้องกับการเปลี่ยนแปลงในสถานะการรวมตัวของสสาร (แข็ง, ของเหลว, ก๊าซ) และคุณสมบัติทางกายภาพอื่นๆ (สี, ความหนาแน่น, แม่เหล็กฯลฯ)
การเปลี่ยนแปลงทางกายภาพมักจะย้อนกลับได้เนื่องจากเปลี่ยนแปลงรูปร่างหรือสถานะของสสาร แต่ไม่ใช่องค์ประกอบของสสาร เช่น เวลาต้ม น้ำ เราสามารถเปลี่ยนของเหลวให้เป็นแก๊สได้ แต่ไอที่เกิดขึ้นนั้นยังประกอบด้วยโมเลกุลของน้ำ หากเราแช่แข็งน้ำ น้ำก็จะเข้าสู่สถานะของแข็ง แต่ยังคงเป็นสารเคมีชนิดเดียวกัน
การเปลี่ยนแปลงทางเคมีเปลี่ยนแปลงการกระจายและการยึดติดของ อะตอม ของสสาร จนได้มารวมกันเป็นอย่างอื่น จึงได้สารที่ต่างไปจากเดิม แม้จะเหมือนกันเสมอ สัดส่วนเนื่องจากสสารไม่สามารถสร้างหรือทำลายได้ มีเพียงการเปลี่ยนแปลงเท่านั้น
ตัวอย่างเช่น ถ้าเราทำปฏิกิริยากับน้ำ (H2O) และโพแทสเซียม (K) เราจะได้สารใหม่สองชนิด ได้แก่ โพแทสเซียมไฮดรอกไซด์ (KOH) และไฮโดรเจน (H2) นี่เป็นปฏิกิริยาที่ปกติแล้วจะปล่อยพลังงานออกมาเป็นจำนวนมาก จึงเป็นอันตรายอย่างยิ่ง
ลักษณะของปฏิกิริยาเคมี
ปฏิกิริยาเคมีมักเป็นกระบวนการที่ไม่สามารถย้อนกลับได้ กล่าวคือ เกี่ยวข้องกับการก่อตัวหรือการทำลาย การเชื่อมโยงทางเคมี ระหว่าง โมเลกุล ของรีเอเจนต์ทำให้เกิดการสูญเสียหรือได้รับพลังงาน
ในปฏิกิริยาเคมี สสารมีการเปลี่ยนแปลงอย่างล้ำลึก แม้ว่าบางครั้งการจัดองค์ประกอบใหม่นี้ไม่สามารถมองเห็นได้ด้วยตาเปล่า ถึงกระนั้นก็สามารถวัดสัดส่วนของสารตั้งต้นได้ ซึ่งจัดการโดยปริมาณสัมพันธ์
ในทางกลับกัน ปฏิกิริยาเคมีจะสร้างผลิตภัณฑ์บางอย่างขึ้นอยู่กับลักษณะของสารตั้งต้น แต่ยังขึ้นอยู่กับสภาวะที่เกิดปฏิกิริยาด้วย
ปัญหาสำคัญอีกประการหนึ่งในปฏิกิริยาเคมีคือความเร็วที่เกิดขึ้น เนื่องจากการควบคุมความเร็วเป็นสิ่งสำคัญสำหรับการใช้งานใน อุตสาหกรรม, ยา ฯลฯ ในแง่นี้ มีวิธีการเพิ่มหรือลดความเร็วของปฏิกิริยาเคมี
ตัวอย่างคือการใช้ตัวเร่งปฏิกิริยา สารที่เพิ่มความเร็วของปฏิกิริยาเคมี สารเหล่านี้ไม่ได้มีส่วนร่วมในปฏิกิริยา แต่จะควบคุมเฉพาะอัตราที่เกิดขึ้นเท่านั้น นอกจากนี้ยังมีสารที่เรียกว่าสารยับยั้ง ซึ่งใช้ในลักษณะเดียวกัน แต่ให้ผลตรงกันข้าม กล่าวคือ พวกมันจะชะลอปฏิกิริยา
ปฏิกิริยาเคมีแสดงอย่างไร?
ปฏิกิริยาเคมีแสดงด้วยสมการเคมี กล่าวคือ สูตร ซึ่งอธิบายรีเอเจนต์ที่เข้าร่วมและผลิตภัณฑ์ที่ได้รับ ซึ่งมักจะระบุเงื่อนไขบางประการโดยธรรมชาติของปฏิกิริยา เช่น การปรากฏตัวของความร้อน ตัวเร่งปฏิกิริยา แสง ฯลฯ
สมการเคมีแรกในประวัติศาสตร์ถูกวาดขึ้นในปี ค.ศ. 1615 โดย Jean Begin ในบทความแรกเรื่อง เคมี, ที่ ไทโรซิเนียม ชิมิคัม วันนี้มีการสอนทั่วไปและต้องขอบคุณพวกเขา เราจึงสามารถเห็นภาพสิ่งที่เกิดขึ้นในปฏิกิริยาบางอย่างได้ง่ายขึ้น
วิธีทั่วไปในการแทนสมการเคมีคือ:
ที่ไหน:
- A และ B เป็นสารตั้งต้น
- C และ D เป็นผลิตภัณฑ์
- ถึง, ข, ค Y d คือสัมประสิทธิ์ปริมาณสัมพันธ์ (เป็นตัวเลขที่ระบุปริมาณของสารตั้งต้นและผลิตภัณฑ์) ที่ต้องปรับเพื่อให้มีปริมาณเท่ากันของแต่ละองค์ประกอบในสารตั้งต้นและในผลิตภัณฑ์ ด้วยวิธีนี้ กฎการอนุรักษ์มวลจึงสำเร็จ (ซึ่งกำหนดว่า มวล ไม่ได้ถูกสร้างหรือถูกทำลาย มีแต่เปลี่ยนรูป)
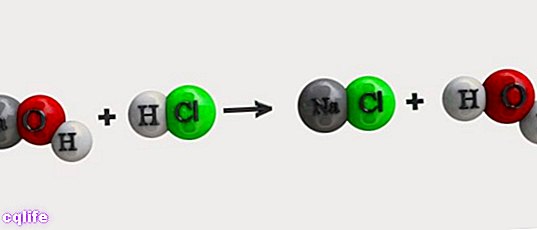
ประเภทและตัวอย่างปฏิกิริยาเคมี
ปฏิกิริยาเคมีสามารถจำแนกได้ตามชนิดของสารตั้งต้นที่ทำปฏิกิริยา จากสิ่งนี้ ปฏิกิริยาเคมีอนินทรีย์และปฏิกิริยาเคมีอินทรีย์สามารถแยกแยะได้ แต่ก่อนอื่น สิ่งสำคัญคือต้องรู้สัญลักษณ์บางอย่างที่ใช้แทนปฏิกิริยาเหล่านี้ผ่านสมการทางเคมี:
ปฏิกิริยาอนินทรีย์ มีส่วนร่วม สารประกอบอนินทรีย์และสามารถจำแนกได้ดังนี้
- ตามประเภทของการเปลี่ยนแปลง
- ปฏิกิริยาสังเคราะห์หรือเติม สารสองชนิดรวมกันทำให้เกิดสารที่แตกต่างกัน ตัวอย่างเช่น:
- ปฏิกิริยาการสลายตัว สารแตกตัวเป็นส่วนประกอบอย่างง่าย หรือสารหนึ่งทำปฏิกิริยากับอีกสารหนึ่งและแตกตัวเป็นสารอื่นๆ ที่มีส่วนประกอบอยู่ ตัวอย่างเช่น:
- ปฏิกิริยาการกระจัดหรือการทดแทน สารประกอบหรือองค์ประกอบแทนที่องค์ประกอบอื่นในสารประกอบ แทนที่มันและปล่อยให้เป็นอิสระ ตัวอย่างเช่น:
- ปฏิกิริยาการแทนที่สองครั้ง สารตั้งต้นสองชนิดแลกเปลี่ยนสารประกอบหรือ องค์ประกอบทางเคมี พร้อมกัน ตัวอย่างเช่น:
- ปฏิกิริยาสังเคราะห์หรือเติม สารสองชนิดรวมกันทำให้เกิดสารที่แตกต่างกัน ตัวอย่างเช่น:
- ตามชนิดและรูปแบบของพลังงานที่แลกเปลี่ยน
- ปฏิกิริยาดูดความร้อน. ความร้อนจะถูกดูดกลืนจนเกิดปฏิกิริยา ตัวอย่างเช่น:
- ปฏิกิริยาคายความร้อน. ความร้อนจะหายไปเมื่อเกิดปฏิกิริยา ตัวอย่างเช่น:
- ปฏิกิริยาเอนโดลูมินัส จำเป็น แสงสว่าง เพื่อให้เกิดปฏิกิริยา ตัวอย่างเช่น: การสังเคราะห์ด้วยแสง.
- ปฏิกิริยาภายนอก แสงจะดับเมื่อเกิดปฏิกิริยา ตัวอย่างเช่น:
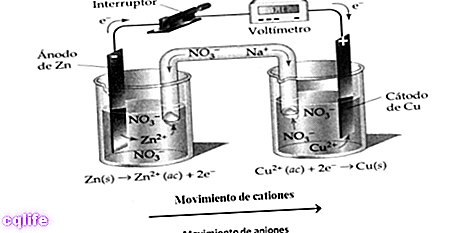
- ปฏิกิริยาเอนโดอิเล็กทริก จำเป็น พลังงานไฟฟ้า เพื่อให้เกิดปฏิกิริยา ตัวอย่างเช่น:
- ปฏิกิริยาเอ็กโซอิเล็กทริก พลังงานไฟฟ้าถูกปล่อยออกมาหรือสร้างขึ้นเมื่อเกิดปฏิกิริยา ตัวอย่างเช่น:
- ปฏิกิริยาดูดความร้อน. ความร้อนจะถูกดูดกลืนจนเกิดปฏิกิริยา ตัวอย่างเช่น:
- ตามความเร็วของปฏิกิริยา
- ปฏิกิริยาช้า ปริมาณรีเอเจนต์ที่บริโภคและปริมาณของผลิตภัณฑ์ที่เกิดขึ้นในช่วงเวลาหนึ่งมีน้อยมาก ตัวอย่างเช่น การเกิดออกซิเดชันของเหล็ก มันเป็นปฏิกิริยาช้า ซึ่งเราเห็นเป็นประจำทุกวันในวัตถุที่เป็นเหล็กที่เป็นสนิม ถ้าปฏิกิริยานี้ไม่ช้า เราก็ไม่มีโครงสร้างเหล็กที่เก่ามากในโลกปัจจุบัน
- ปฏิกิริยาตอบสนองอย่างรวดเร็ว ปริมาณรีเอเจนต์ที่บริโภคและปริมาณของผลิตภัณฑ์ที่เกิดขึ้นในช่วงเวลาที่กำหนดนั้นดีมาก ตัวอย่างเช่น ปฏิกิริยาของโซเดียมกับน้ำเป็นปฏิกิริยาที่อันตรายมาก นอกจากจะเกิดอย่างรวดเร็วแล้ว
- ปฏิกิริยาช้า ปริมาณรีเอเจนต์ที่บริโภคและปริมาณของผลิตภัณฑ์ที่เกิดขึ้นในช่วงเวลาหนึ่งมีน้อยมาก ตัวอย่างเช่น การเกิดออกซิเดชันของเหล็ก มันเป็นปฏิกิริยาช้า ซึ่งเราเห็นเป็นประจำทุกวันในวัตถุที่เป็นเหล็กที่เป็นสนิม ถ้าปฏิกิริยานี้ไม่ช้า เราก็ไม่มีโครงสร้างเหล็กที่เก่ามากในโลกปัจจุบัน
- ตามชนิดของอนุภาคที่เกี่ยวข้อง
- ปฏิกิริยา กรดเบส. โอนแล้ว โปรตอน (ส+). ตัวอย่างเช่น:
- ปฏิกิริยาออกซิเดชัน-รีดักชัน โอนแล้ว อิเล็กตรอน. ในปฏิกิริยาประเภทนี้ เราต้องดูที่เลขออกซิเดชันของธาตุที่เกี่ยวข้อง ถ้าเลขออกซิเดชันของธาตุเพิ่มขึ้น ธาตุนั้นจะถูกออกซิไดซ์ ถ้าลดลง ธาตุนั้นจะลดลง ตัวอย่างเช่น: ในปฏิกิริยานี้ เหล็กจะถูกออกซิไดซ์และโคบอลต์จะลดลง
- ปฏิกิริยา กรดเบส. โอนแล้ว โปรตอน (ส+). ตัวอย่างเช่น:
- ตามทิศทางของปฏิกิริยา
- ปฏิกิริยาย้อนกลับ พวกมันไปทั้งสองทาง นั่นคือ ผลิตภัณฑ์สามารถกลายเป็นสารตั้งต้นได้อีกครั้ง ตัวอย่างเช่น:
- ปฏิกิริยาที่ไม่สามารถย้อนกลับได้ เกิดขึ้นในแง่เดียวเท่านั้น กล่าวคือ สารตั้งต้นถูกแปรสภาพเป็นผลิตภัณฑ์และกระบวนการที่ตรงกันข้ามจะไม่เกิดขึ้น ตัวอย่างเช่น:
- ปฏิกิริยาย้อนกลับ พวกมันไปทั้งสองทาง นั่นคือ ผลิตภัณฑ์สามารถกลายเป็นสารตั้งต้นได้อีกครั้ง ตัวอย่างเช่น:
ปฏิกิริยาอินทรีย์ พวกเขาเกี่ยวข้องกับสารประกอบอินทรีย์ซึ่งเกี่ยวข้องกับพื้นฐานของชีวิต ขึ้นอยู่กับชนิดของสารประกอบอินทรีย์สำหรับการจำแนกประเภท เนื่องจากแต่ละกลุ่มฟังก์ชันมีปฏิกิริยาเฉพาะช่วง ตัวอย่างเช่น แอลเคน แอลคีน แอลไคน์ แอลกอฮอล์, คีโตน, อัลดีไฮด์, อีเทอร์, เอสเทอร์, ไนไตรล์ ฯลฯ
ตัวอย่างปฏิกิริยาของสารประกอบอินทรีย์ ได้แก่
- ฮาโลเจนของอัลเคน ไฮโดรเจนของอัลเคนถูกแทนที่ด้วยฮาโลเจนที่สอดคล้องกัน
- การเผาไหม้ของแอลเคน อัลเคนทำปฏิกิริยากับออกซิเจนเพื่อให้ คาร์บอนไดออกไซด์ และน้ำ ปฏิกิริยาประเภทนี้จะปล่อยพลังงานออกมาเป็นจำนวนมาก
- ฮาโลเจนของแอลคีน ไฮโดรเจนสองชนิดที่มีอยู่ในคาร์บอนซึ่งก่อพันธะคู่จะถูกแทนที่
- ไฮโดรจีเนชันของแอลคีน ไฮโดรเจนสองชนิดถูกเติมลงในพันธะคู่ ทำให้เกิดอัลเคนที่สอดคล้องกัน ปฏิกิริยานี้เกิดขึ้นต่อหน้าตัวเร่งปฏิกิริยา เช่น แพลตตินั่ม แพลเลเดียม หรือนิกเกิล
ความสำคัญของปฏิกิริยาเคมี
ทั้งการสังเคราะห์ด้วยแสงและการหายใจเป็นตัวอย่างของปฏิกิริยาเคมีปฏิกิริยาเคมีเป็นพื้นฐานของการดำรงอยู่และความเข้าใจของโลกอย่างที่เราทราบ การเปลี่ยนแปลงที่เกิดขึ้นภายใต้สภาวะธรรมชาติหรือที่มนุษย์สร้างขึ้น (และมักจะสร้างวัสดุที่มีคุณค่า) เป็นเพียงตัวอย่างเดียวเท่านั้น หลักฐานที่สำคัญที่สุดของความสำคัญของปฏิกิริยาเคมีคือตัวมันเอง ในทุกการแสดงออก
การมีอยู่ของ สิ่งมีชีวิต ทุกชนิดเป็นไปได้ด้วยความสามารถในการทำปฏิกิริยาของสสาร ซึ่งทำให้รูปแบบเซลล์แรกของชีวิตแลกเปลี่ยนพลังงานกับสิ่งแวดล้อมผ่านเส้นทางเมแทบอลิซึม นั่นคือผ่านลำดับของปฏิกิริยาเคมีที่ให้พลังงานที่มีประโยชน์มากกว่าที่บริโภคเข้าไป
ตัวอย่างเช่นในชีวิตประจำวันของเรา การหายใจ ประกอบด้วยปฏิกิริยาเคมีหลายอย่างซึ่งมีอยู่ใน การสังเคราะห์ด้วยแสง ของ พืช.
ความเร็วของปฏิกิริยาเคมี
ปฏิกิริยาเคมีต้องใช้เวลาตามที่กำหนดไว้จึงจะเกิดขึ้น ซึ่งแตกต่างกันไปขึ้นอยู่กับลักษณะของสารตั้งต้นและสภาพแวดล้อมที่เกิดปฏิกิริยา
ปัจจัยที่ส่งผลต่ออัตราการเกิดปฏิกิริยาเคมีโดยทั่วไป ได้แก่
- อุณหภูมิสูงขึ้น อุณหภูมิที่สูงมักจะเพิ่มความเร็วของปฏิกิริยาเคมี
- ความดันที่เพิ่มขึ้น การเพิ่มความดันมักจะเพิ่มความเร็วของปฏิกิริยาเคมี โดยทั่วไปจะเกิดขึ้นเมื่อสารที่มีความไวต่อการเปลี่ยนแปลงความดัน เช่น ก๊าซ ทำปฏิกิริยา ในกรณีของของเหลวและของแข็ง การเปลี่ยนแปลงของแรงดันจะไม่ทำให้เกิดการเปลี่ยนแปลงที่สำคัญในอัตราของปฏิกิริยา
- สถานะการรวมตัวซึ่งมีรีเอเจนต์อยู่ ของแข็งมีแนวโน้มที่จะทำปฏิกิริยาช้ากว่าของเหลวหรือก๊าซ แม้ว่าความเร็วจะขึ้นอยู่กับปฏิกิริยาของสารแต่ละชนิดด้วย
- การใช้ตัวเร่งปฏิกิริยา (สารที่ใช้เพื่อเพิ่มความเร็วของปฏิกิริยาเคมี) สารเหล่านี้ไม่ได้มีส่วนร่วมในปฏิกิริยา แต่จะควบคุมเฉพาะอัตราที่เกิดขึ้นเท่านั้น นอกจากนี้ยังมีสารที่เรียกว่าสารยับยั้ง ซึ่งใช้ในลักษณะเดียวกัน แต่ให้ผลตรงกันข้าม กล่าวคือ พวกมันจะชะลอปฏิกิริยา
- พลังงานส่องสว่าง (Light) ปฏิกิริยาเคมีบางอย่างจะเร่งขึ้นเมื่อแสงส่องมาที่พวกมัน
- ความเข้มข้นของรีเอเจนต์ ปฏิกิริยาเคมีส่วนใหญ่จะเกิดขึ้นเร็วขึ้นหากมีรีเอเจนต์ที่มีความเข้มข้นสูง

