เราอธิบายว่าการกลั่นคืออะไร ตัวอย่างของวิธีการแยกนี้และประเภทของการกลั่นที่สามารถใช้ได้

การกลั่นคืออะไร?
การกลั่นเรียกว่าวิธีการแยกเฟสซึ่งเป็นหนึ่งใน วิธีการแยกสารผสม. การกลั่นประกอบด้วยการใช้กระบวนการทางกายภาพสองขั้นตอนติดต่อกันและควบคุม: การทำให้กลายเป็นไอ และ การควบแน่นโดยเลือกใช้เฉพาะเพื่อแยกส่วนประกอบของ a ส่วนผสม มักจะมีลักษณะเป็นเนื้อเดียวกัน กล่าวคือ ส่วนประกอบไม่สามารถแยกแยะได้ด้วยตาเปล่า
ของผสมที่สามารถแยกออกเป็นส่วนประกอบแต่ละส่วนได้โดยใช้การกลั่นสามารถประกอบด้วยสอง ของเหลว, แ แข็ง ในของเหลวหรือแม้กระทั่ง ก๊าซ สมูทตี้ วิธีการแยกนี้ขึ้นอยู่กับความแตกต่างของจุดเดือด (คุณสมบัติโดยธรรมชาติของ วัตถุ, อะไรคือ อุณหภูมิ ซึ่ง ความดัน ไอของของเหลวเท่ากับความดันรอบ ๆ ของเหลว) ของสารต่างๆ สารที่มีค่าต่ำสุด จุดเดือด มีแล้วสารนี้จะควบแน่นในภาชนะอื่นและจะค่อนข้างบริสุทธิ์
ด้วยวิธีนี้เพื่อให้การกลั่นเป็นไปอย่างถูกวิธี เราต้องต้มส่วนผสมให้เดือดจนถึงจุดเดือดของตัวใดตัวหนึ่ง สาร ส่วนประกอบต่างๆ ซึ่งจะกลายเป็นไอและสามารถนำไปบรรจุในภาชนะที่เย็นลง ซึ่งจะทำให้เกิดการควบแน่นและกลายเป็นของเหลวอีกครั้ง
ในทางกลับกัน สารที่เป็นส่วนประกอบอื่นๆ จะยังคงอยู่ในภาชนะโดยไม่มีการดัดแปลงใดๆ แต่ทั้งสองกรณีเราจะมี สารบริสุทธิ์, ฟรีจากการผสมเริ่มต้น
กฎของราอูลท์
เมื่อเรามีส่วนผสมของของเหลวในอุดมคติ (ส่วนผสมที่ปฏิกิริยาระหว่าง อนุภาค ต่างกันถือว่าเท่ากับปฏิสัมพันธ์ระหว่างอนุภาคที่เท่ากัน) กฎของ Raoult ได้รับการเติมเต็ม
กฎหมายฉบับนี้ระบุว่าแรงดันไอบางส่วนของส่วนประกอบแต่ละอย่างในส่วนผสมของแก๊สมีค่าเท่ากับแรงดันไอของส่วนประกอบบริสุทธิ์คูณด้วยเศษส่วนของโมลในส่วนผสมของเหลว
ความดันไอรวมคือผลรวมของแรงดันบางส่วนของส่วนประกอบของของผสมในเฟสแก๊ส ในทางกลับกัน เศษส่วนโมลของส่วนประกอบในส่วนผสมเป็นตัววัดความเข้มข้นของมันอย่างไร้มิติ ขนาดที่กล่าวถึงข้างต้นสามารถคำนวณได้โดยใช้สมการต่อไปนี้:
ที่ไหน:
- px Y พาย คือความดันบางส่วนของส่วนประกอบ x และ Y ตามลำดับในส่วนผสมของไอระเหยที่อยู่รอบๆ ส่วนผสมของของเหลว
- px * และ py * คือความดันไอของส่วนประกอบ x และ ย.
- xx Y xy เป็นเศษส่วนโมลของส่วนประกอบ x และ Y ในส่วนผสมของเหลว
- nx Y ny คือปริมาณสารของส่วนประกอบ x และ Y ในส่วนผสมของเหลว
กฎของ Raoult ที่ยกมาข้างต้นใช้ได้กับสารผสมในอุดมคติ (ซึ่งเป็นแบบจำลองที่มนุษย์กำหนดขึ้นเพื่อทำให้การศึกษาง่ายขึ้น) แต่ในความเป็นจริง กฎข้อนี้จะได้รับผลกระทบเมื่อส่วนผสมนั้นเป็นของจริง
ดังนั้น หากอนุภาคที่แตกต่างกันในส่วนผสมมีแรงระหว่างโมเลกุลที่แรงกว่าอนุภาคในของเหลวบริสุทธิ์ ความดันไอของส่วนผสมจะน้อยกว่าความดันไอของของเหลวบริสุทธิ์ ซึ่งทำให้เกิดการเบี่ยงเบนเชิงลบจากกฎของราอูลท์
ในทางกลับกัน หากแรงระหว่างโมเลกุลระหว่างอนุภาคในของเหลวบริสุทธิ์มีค่ามากกว่าอนุภาคในส่วนผสม อนุภาคในส่วนผสมจะสามารถหลบหนีไปยังเฟสไอได้ง่ายขึ้นเพื่อให้แรงดันไอ ของส่วนผสมจะมากขึ้นทำให้เกิดการเบี่ยงเบนเชิงบวกจากกฎของราอูลท์
เมื่อคุณต้องการกลั่นส่วนผสมอะซีโอโทรปิก (เช่น เอทานอลและน้ำ) จำเป็นต้องเติมส่วนประกอบบางส่วน (เบนซีนในกรณีนี้) เพื่อให้อะซีโอโทรปมีการปรับเปลี่ยนและในลักษณะนี้เพื่อให้สามารถแยกส่วนประกอบของ ส่วนผสม อะซีโอโทรปคือของผสมของเหลวที่มีองค์ประกอบที่กำหนดไว้ว่าเมื่อเดือด ไอระเหยที่เกิดขึ้นจะมีองค์ประกอบของส่วนผสมเหมือนกัน (ดังนั้น ส่วนประกอบของส่วนผสมอะซีโอโทรปิกจึงไม่สามารถแยกออกได้ด้วยการกลั่นแบบธรรมดาหรือแบบเศษส่วน)
Azeotropes มีอุณหภูมิการเดือดที่กำหนดไว้ ตัวอย่างเช่น ที่ความดัน 1 atm เอทานอลเดือดที่ 78.37 ° C และน้ำเดือดที่ 100 ° C ในขณะที่ Azeotrope ในน้ำเอทานอลเดือดที่ 78.2 ° C สารผสม Azeotropic มีการเบี่ยงเบนเชิงลบหรือบวกจากกฎของ Raoult แล้วแต่กรณี
ประเภทของการกลั่น
การกลั่นอาจเกิดขึ้นได้หลายวิธี:
- การกลั่นอย่างง่าย ขั้นแรกสุดจะประกอบด้วยการต้มส่วนผสมจนส่วนผสมต่างๆ แยกออกจากกัน เป็นวิธีการแยกสารที่มีประสิทธิภาพเมื่อจุดเดือดของส่วนประกอบของส่วนผสมต่างกันมาก (ตามหลักแล้วควรมีความแตกต่างอย่างน้อย 25 ° C มิฉะนั้นจะไม่รับประกันความบริสุทธิ์ทั้งหมดของสารกลั่น)
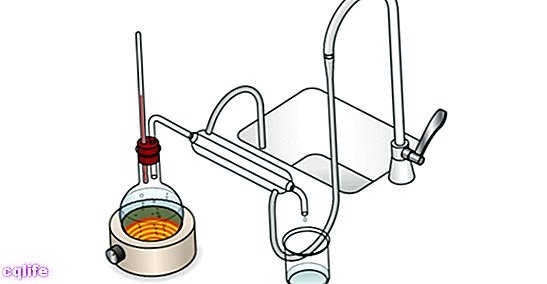
- การกลั่นแบบเศษส่วน ดำเนินการโดยใช้คอลัมน์การแยกส่วน ซึ่งประกอบด้วยแผ่นต่างๆ ซึ่งการกลายเป็นไอและการควบแน่นเกิดขึ้นอย่างต่อเนื่อง เพื่อรับประกันความบริสุทธิ์ที่มากขึ้นในส่วนประกอบที่แยกจากกัน
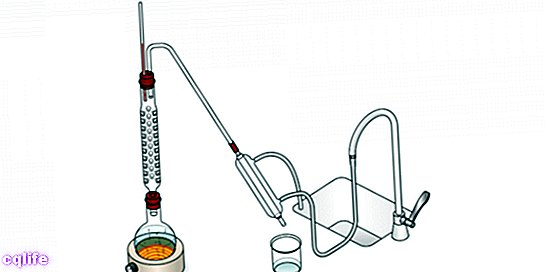
- การกลั่นด้วยสุญญากาศ โดยการลดแรงดันจนเกิดสุญญากาศ กระบวนการจะถูกเร่งปฏิกิริยาเพื่อลดจุดเดือดของส่วนประกอบ เนื่องจากบางส่วนมีจุดเดือดสูงมากซึ่งสามารถลดลงได้เมื่อแรงดันลดลงอย่างมาก และด้วยเหตุนี้จึงเร่งกระบวนการกลั่น
- การกลั่นอะซีโอทรอปิก เป็นการกลั่นที่จำเป็นในการทำลายอะซีโอโทรป นั่นคือ ส่วนผสมที่มีสารทำหน้าที่เป็นหนึ่ง แม้กระทั่งจุดเดือดร่วมกัน ดังนั้นจึงไม่สามารถแยกออกจากการกลั่นแบบธรรมดาหรือแบบเศษส่วนได้ ในการแยกส่วนผสมอะซีโอทรอปิก จำเป็นต้องปรับเปลี่ยนสภาวะการผสม เช่น โดยการเพิ่มส่วนประกอบแยกบางส่วน
- การกลั่นด้วยไอน้ำ ส่วนประกอบที่ระเหยได้และไม่ระเหยของส่วนผสมจะถูกแยกออกจากกันโดยการฉีดไอน้ำโดยตรง
- การกลั่นแบบแห้ง ประกอบด้วยวัสดุแข็งที่ให้ความร้อนโดยไม่มี ตัวทำละลาย ของเหลว ได้ก๊าซแล้วควบแน่นในภาชนะอื่น
- ปรับปรุงการกลั่น เรียกอีกอย่างว่าการกลั่นแบบทางเลือกหรือแบบรีแอกทีฟ โดยจะปรับให้เข้ากับกรณีเฉพาะของสารผสมที่แยกออกได้ยากหรือมีจุดเดือดเหมือนกัน
ตัวอย่างของการกลั่น

- การกลั่นน้ำมัน การแยกจากกันต่างๆ ไฮโดรคาร์บอน ที่มีอยู่ใน ปิโตรเลียม ดำเนินการโดยการกลั่นแบบเศษส่วน การจัดเก็บในชั้นต่างๆ หรือช่องแยกของคอลัมน์การกลั่น ซึ่งแต่ละสารประกอบที่ได้มาจากการปรุงน้ำมันดิบ ก๊าซเหล่านี้ลอยขึ้นและควบแน่นในชั้นบนของเสา ในขณะที่สารที่มีความหนาแน่นมากกว่า เช่น แอสฟัลต์และพาราฟินยังคงอยู่ในชั้นล่าง
- การแตกตัวเร่งปฏิกิริยา นี่คือชื่อที่กำหนดให้กับการกลั่นด้วยสุญญากาศตามปกติในกระบวนการผลิตน้ำมัน โดยใช้เสาสุญญากาศเพื่อแยกก๊าซออกจากการปรุงอาหารแบบดิบ ดังนั้นการเดือดของไฮโดรคาร์บอนจะถูกเร่งและ กระบวนการ. การแคร็กเป็นประเภทของการกลั่นแบบทำลายล้าง ซึ่งไฮโดรคาร์บอนที่มีขนาดใหญ่กว่าจะแตกตัว (ที่อุณหภูมิสูงและใช้ตัวเร่งปฏิกิริยา) ให้เป็นไฮโดรคาร์บอนที่มีขนาดเล็กกว่าซึ่งมีจุดเดือดต่ำกว่า
- การทำให้บริสุทธิ์เอทานอล ที่จะแยกออก แอลกอฮอล์ เช่นเดียวกับเอทานอลจากน้ำในระหว่างการผลิตในห้องปฏิบัติการ ใช้การกลั่นด้วยอะซีโอทรอปิก เติมน้ำมันเบนซินผสมหรือส่วนประกอบอื่นๆ ที่ส่งเสริมหรือเร่งการแยกสาร และสามารถกำจัดออกได้ง่ายโดยไม่เปลี่ยนแปลงองค์ประกอบทางเคมีของ ผลิตภัณฑ์.
- การแปรรูปถ่านหิน เพื่อให้ได้เชื้อเพลิงอินทรีย์เหลว ถ่านหินหรือไม้จะถูกใช้โดยวิธีการกลั่นแบบแห้ง ดังนั้นก๊าซที่ปล่อยออกมาใน การเผาไหม้.
- เทอร์โมไลซิสของเกลือแร่ โดยการกลั่นแบบแห้ง จะได้สารแร่ต่างๆ ที่เป็นประโยชน์ทางอุตสาหกรรมสูง จากการกลั่นและการควบแน่นของก๊าซที่ได้จากการเผาเกลือแร่
- อัลเลมบิก. นี่คือชื่อที่มอบให้กับอุปกรณ์ที่ประดิษฐ์ขึ้นในสมัยโบราณของอาหรับ ซึ่งมีวัตถุประสงค์เพื่อผลิตน้ำหอม ยารักษาโรค และแอลกอฮอล์จากผลไม้หมัก ในการปฏิบัติการ ใช้หลักการกลั่น: สารถูกทำให้ร้อนในหม้อต้มขนาดเล็ก และก๊าซที่ผลิตได้จะถูกทำให้เย็นลงในขดลวดที่นำไปสู่ภาชนะอื่นซึ่งของเหลวที่เกิดจากการควบแน่นของก๊าซดังกล่าวจะถูกรวบรวม
- การผลิตน้ำหอม การกลั่นด้วยไอน้ำใช้เพื่อให้ได้น้ำหอม น้ำเดือดร่วมกับดอกไม้ที่เก็บรักษาไว้ เพื่อผลิตก๊าซที่มีกลิ่นที่ต้องการ และเมื่อควบแน่นแล้ว สามารถใช้เป็นของเหลวพื้นฐานในน้ำหอมได้


